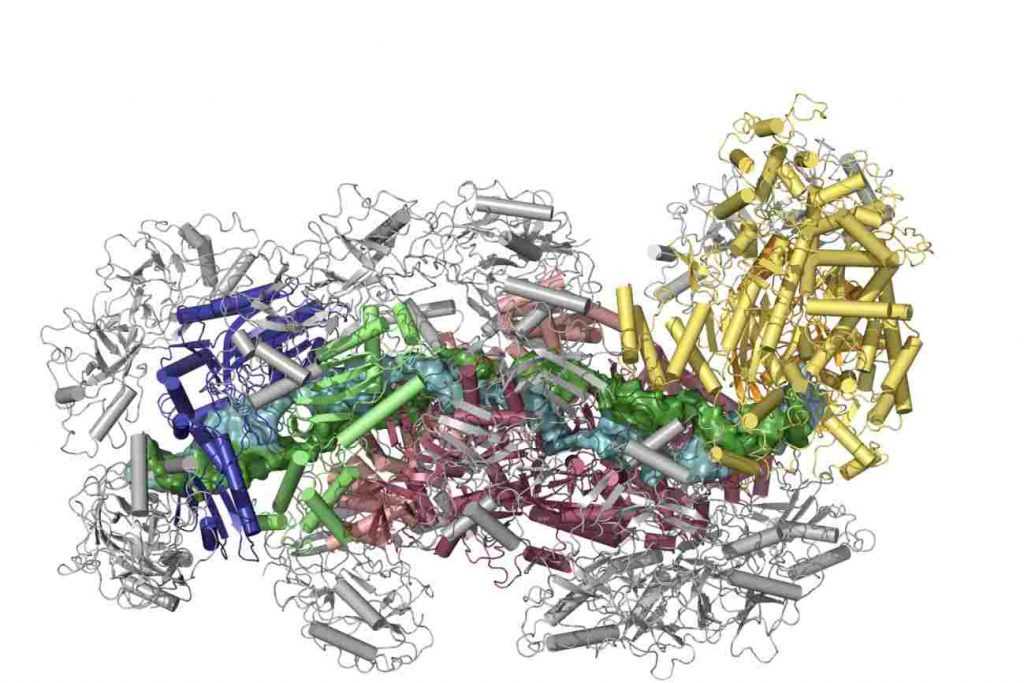
Investigadores de la Universidad de Copenhague, liderados por el español Guillermo Montoya, han descrito la estructura atómica de Cmr-β, el sistema CRISPR Cas de mayor tamaño y complejidad.
Además, han observado cómo funciona su respuesta inmunitaria contra los fagos invasores de las bacterias. El hallazgo podría tener aplicaciones futuras en la lucha contra la resistencia a los antibióticos.

Ana Hernando
Un equipo liderado por el biólogo molecular español Guillermo Montoya en la Novo Nordisk Foundation Center for Protein Research, en la Universidad de Copenhague, ha logrado determinar y analizar la estructura atómica del sistema CRISPR más complejo y de mayor tamaño conocido hasta ahora.
El sistema, descrito en un estudio que se publica en la revista Molecular Cell, se denomina Cmr-β y pertenece al subgrupo CRISPR Cas tipo III-B. Los investigadores han utilizado una tecnología avanzada de criomicroscopía electrónica (CryoEM) para mapearlo.
CRIPSPR Cas Cmr-β puede “eliminar el ARN del invasor específicamente y el ADN y ARN de una sola hebra de manera inespecífica, por lo tanto, funciona como una trituradora de ácidos nucleicos”, dice Montoya
«Hemos resuelto el mayor y más complicado sistema CRISPR Cas visto hasta ahora que elimina el material genético de virus bacterianos u otro tipo de invasores. Gracias a esta información, hemos logrado entender cómo funciona a nivel molecular», dice Montoya a SINC.
CRIPSPR Cas Cmr-β puede, entre otras cosas, “eliminar el ARN del invasor específicamente y el ADN y ARN de una sola hebra de manera inespecífica, por lo tanto, funciona como una trituradora de ácidos nucleicos”, señala.
El investigador aclara que “será muy difícil que este complejo proteico pueda ser usado para la edición de genes como se hace con las famosas tijeras moleculares CRISPR Cas9, debido a su complejidad y a su tamaño, ya que es alrededor de cinco veces mayor”.
Sin embargo, opina que en el futuro este sistema “podría ser clave para entender la respuesta inmunitaria de las bacterias y tener aplicación en la lucha contra la resistencia a los antibióticos”.
Lucha contra los fagos invasores
CRISPR se encuentra en organismos procariotas (bacterias y arqueobacterias) y está involucrado en su sistema inmunitario, donde tiene una función clave en la constante lucha contra los fagos invasores, virus específicos de bacterias.
“En el futuro, podríamos ser capaces de utilizar este sistema CRISPR para el diagnóstico de problemas de salud que hasta el momento se nos escapaban», destaca el investigador
En el nuevo estudio, Montoya y su equipo han investigado los mecanismos detrás de la respuesta inmunitaria de Cmr-β contra estos fagos y cómo se regula.
«Nuestros hallazgos destacan las diversas estrategias de defensa de la familia CRISPR de tipo III. También hemos identificado una subunidad única llamada Cmr7, que parece controlar la actividad del complejo proteico, y creemos además que puede defenderse contra posibles proteínas virales anti-CRISPR», detalla Nicholas Heelund Sofos, coautor del estudio.
Según Montoya, CRISPR Cas Cmr-β puede tener además potencial terapéutico. “En el futuro, podríamos ser capaces de utilizarlo para el diagnóstico de problemas de salud que hasta el momento se nos escapaban. Ahora, nuestro objetivo es buscar una aplicación para este sistema», concluye.
Una empresa para mejorar el diagnóstico y el tratamiento con CRISPR
Guillermo Montoya, junto con Stefano Stella, uno de los investigadores de su equipo, han creado empresa llamada TwelveBIO. Su objetivo, dicen a SINC, es mejorar la tecnología CRISPR aplicada al diagnóstico y tratamiento de enfermedades.
La nueva compañía, creada a finales de 2019, es una spin off de la Universidad de Copenhague y ha recibido subvenciones de fundaciones danesas de cerca de 500.000 euros para su puesta en marcha.
Montoya explica que la firma está ahora mismo centrada en las posibles aplicaciones en diagnóstico y tratamiento de las tijeras moleculares de edición genética CRISPR-Cas12, que “tiene un gran potencial para la identificación de biomarcadores, como patógenos y mutaciones de cáncer en muestras de pacientes clínicos”, señala.
Por su parte, Stefano Stella indica que “Cas12a es la herramienta de edición de próxima generación, gracias a su mayor especificidad en comparación con la proteína Cas9, que fue la primera enzima CRISPR descubierta en 2012″.
Referencia:
Nicholas Sofos, Mingxia Feng, Stefano Stella, Tillmann Pape, Anders Fuglsang, Jinzhong Lin, Qihong Huang, Yingjun L, Qunxin She, Guillermo Montoya. “Structures of the Cmr-β Complex Reveal the Regulation of the Immunity Mechanism of Type III-B CRISPR-Cas”. Molecular Cell (julio, 2020).
