Los científicos han utilizado técnicas de edición de genes para identificar y cambiar partes del ADN del pollo que podrían limitar la propagación del virus de la gripe aviar en los animales.
por la Universidad de Edimburgo
Los investigadores pudieron restringir, pero no bloquear completamente, que el virus infecte a los pollos alterando una pequeña sección de su ADN.
Las aves no mostraron signos de que el cambio en su ADN tuviera algún impacto en su salud o bienestar.
Los hallazgos son un paso adelante alentador, pero los expertos destacan que se necesitarían más modificaciones genéticas para producir una población de pollos que no pueda ser infectada por la gripe aviar, una de las enfermedades animales más costosas del mundo.
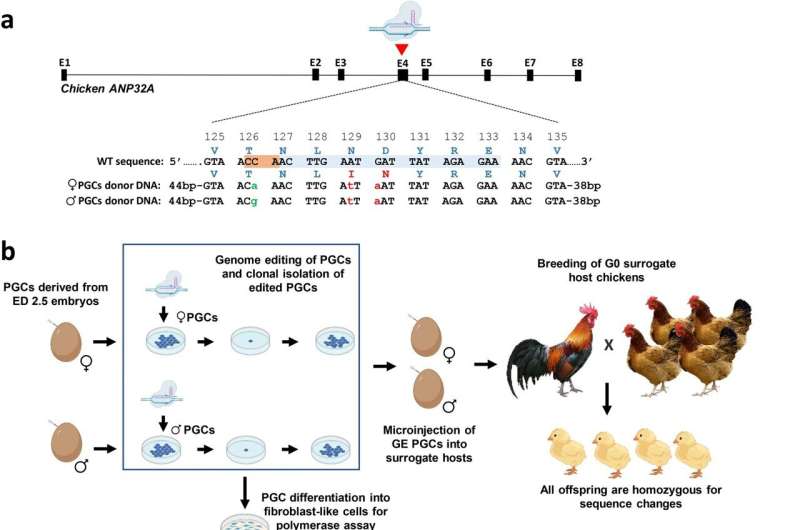
Científicos de la Universidad de Edimburgo, el Imperial College de Londres y el Instituto Pirbright criaron pollos utilizando técnicas de edición de genes para alterar la sección de ADN responsable de producir la proteína ANP32A. Durante una infección, los virus de la gripe secuestran esta molécula para ayudar a replicarse.
Cuando los pollos editados con el gen ANP32A fueron expuestos a una dosis normal de la cepa H9N2-UDL del virus de la influenza aviar, comúnmente conocida como gripe aviar, 9 de cada 10 aves permanecieron no infectadas y no se propagó a otros pollos.
Protección parcial
Luego, el equipo de investigación expuso a las aves genéticamente editadas a una dosis artificialmente alta del virus de la influenza aviar para probar más a fondo su resistencia.
Cuando se expuso a la dosis alta, la mitad del grupo (5 de cada 10 aves) se infectó. Sin embargo, la edición genética proporcionó cierta protección, con la cantidad de virus en los pollos infectados editados genéticamente mucho más bajo que el nivel típicamente observado durante la infección en pollos no editados genéticamente.
La edición genética también ayudó a limitar la propagación del virus a solo uno de los cuatro pollos no modificados genéticamente colocados en la misma incubadora. No hubo transmisión a aves editadas genéticamente.
Evolución viral
Los científicos descubrieron que en las aves editadas con el gen ANP32A, el virus se había adaptado para conseguir el apoyo de dos proteínas relacionadas, ANP32B y ANP32E, para replicarse.
Tras las pruebas de laboratorio , los científicos descubrieron que algunas de las mutaciones permitían al virus utilizar la versión humana de ANP32, pero su replicación seguía siendo baja en cultivos de células de las vías respiratorias humanas.
Los expertos dicen que se necesitarían cambios genéticos adicionales para que el virus infecte y se propague efectivamente en los humanos.
Sin embargo, los hallazgos demuestran que la edición única del gen ANP32A no es lo suficientemente robusta para su aplicación en la producción de pollos, según el equipo.
Otras ediciones
Para prevenir la aparición de virus de escape (virus que se adaptan para evadir la edición genética y causar infección), el equipo de investigación apuntó a continuación a secciones adicionales de ADN responsables de producir las tres proteínas (ANP32A, ANP32B y ANP32E) dentro de células de pollo cultivadas en laboratorio.
En cultivos celulares en el laboratorio, el crecimiento del virus se bloqueó con éxito en células con las tres ediciones genéticas.
El siguiente paso será intentar desarrollar pollos con modificaciones en los tres genes . Aún no se han producido aves.
El estudio destaca la importancia de una edición genética responsable y la necesidad de estar alerta a los riesgos de impulsar la evolución viral en direcciones no deseadas si no se logra una resistencia completa, dicen los expertos.
La gripe aviar es una importante amenaza mundial, con un impacto devastador tanto en las poblaciones de aves silvestres como de granja. Sólo en el Reino Unido, el actual brote de gripe aviar H5N1 ha diezmado las poblaciones de aves marinas y le ha costado a la industria avícola más de £100 millones en pérdidas.
En casos raros, las mutaciones en el virus de la gripe aviar le permiten infectar a las personas y causar enfermedades graves. Se necesitan urgentemente esfuerzos para controlar la propagación de la enfermedad.
«La gripe aviar es una gran amenaza para las poblaciones de aves. La vacunación contra el virus plantea una serie de desafíos, con importantes problemas prácticos y de costos asociados con el despliegue de la vacuna. La edición genética ofrece una ruta prometedora hacia la resistencia permanente a las enfermedades, que podría transmitirse a través de generaciones, protegiendo a las aves de corral y reduciendo los riesgos para los humanos y las aves silvestres. Nuestro trabajo muestra que detener la propagación de la influenza aviar en los pollos necesitará varios cambios genéticos simultáneos», dijo el profesor Mike McGrew, investigador principal del estudio, de la Universidad Roslin de la Universidad de Edimburgo. Instituto.
«Este trabajo es una colaboración apasionante que fusiona nuestra experiencia en virología con la capacidad genética líder en el mundo del Instituto Roslin. Aunque todavía no tenemos la combinación perfecta de ediciones genéticas para llevar este enfoque al campo, los resultados han dicho «Nos enseña mucho sobre cómo funciona el virus de la gripe dentro de la célula infectada y cómo ralentizar su replicación», afirmó la profesora Wendy Barclay, del Imperial College de Londres.
El trabajo se publica en la revista Nature Communications .
Más información: Alewo Idoko-Akoh et al, Creación de resistencia a la infección por influenza aviar mediante la edición del genoma de la familia de genes ANP32, Nature Communications (2023). DOI: 10.1038/s41467-023-41476-3 . www.nature.com/articles/s41467-023-41476-3
